Wetenschappelijke publicaties

Eindelijk een stap vooruit in de behandeling van de secundair progressieve vormen van multiple sclerose!
Op 13 december 2024 wees de Amerikaanse Food and Drug Administration (FDA) het geneesmiddel tolebrutinib aan als ‘doorbraaktherapie’, voor de behandeling van secundair progressieve multiple sclerose zonder opflakkeringen, na afloop van een succesvolle klinische fase 3 studie.
Tolebrutinib, ontwikkeld door de firma Sanofi, is een Bruton's tyrosinekinase (BTK)-remmer. BTK is een enzym dat in 1993 werd ontdekt door Bruton en aanwezig is in de B-lymfocyten, de macrofagen en de microgliacellen van de hersenen. Die laatste cellen zijn de specifieke macrofagen van de hersenen. Tolebrutinib dringt door de bloed-hersenbarrière, en door dit bijzondere enzym te blokkeren, belet het dat zowel de B-lymfocyten als de macrofagen geactiveerd worden.
Die laatste spelen een belangrijke rol in de progressie van de letsels en dus van de symptomen van multiple sclerose zonder klinische opflakkeringen. Ze bevinden zich aan de rand van de actieve chronische plaques en liggen aan de basis van de continue en verraderlijke vernietiging van de myeline-omhulsels, waardoor de demyeliniserende letsels langzaam groter worden (‘chronic expanding lesions’). Ze worden ook geactiveerd door de degeneratie van de zenuwvezels (axonen).

De fase 3 studie met de naam HERCULES omvatte 1131 patiënten in de progressieve fase van hun ziekte, bij wie er gedurende minstens 2 jaar voor het begin van de klinische studie geen opflakkeringen waren geweest. Gemiddeld hadden deze patiënten al 7 jaar geen opflakkering meer vertoond en lag hun invaliditeitsscore (EDSS) tussen 3 (aanzienlijke handicap in een neurologische functie) en 6,5 (kunnen stappen met dubbele ondersteuning over een twintigtal meter). 60% van de patiënten in de studie moesten geholpen worden bij het stappen, wat wijst op de vergevorderde handicap van de onderzochte populatie.
Het belangrijkste resultaat van deze studie was dat werd aangetoond dat tolebrutinib de progressie van de handicap met 31% vertraagt in vergelijking met de placebogroep. Dat verschil is statistisch bijzonder significant. Er was ook bij 10% van de behandelde deelnemers een bevestigde verbetering van de handicap, dat is 2 keer meer dan bij degenen van de placebogroep.
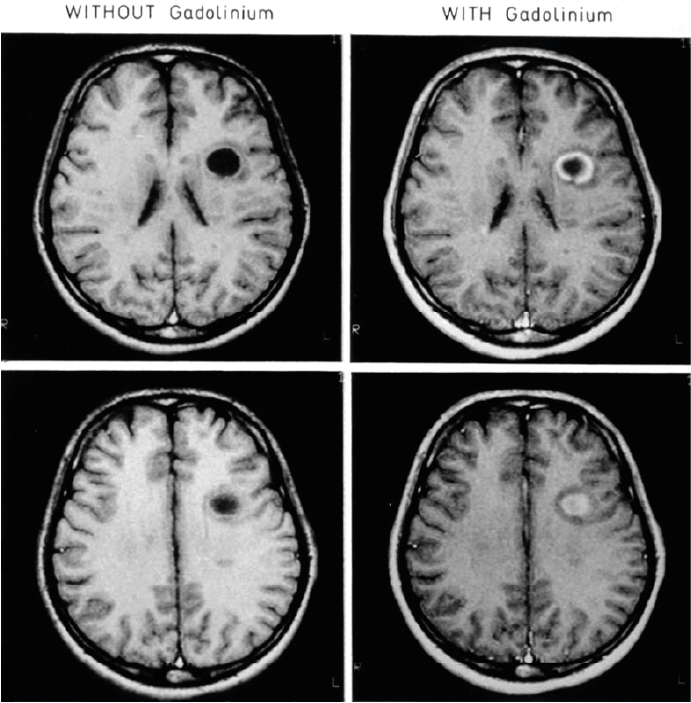
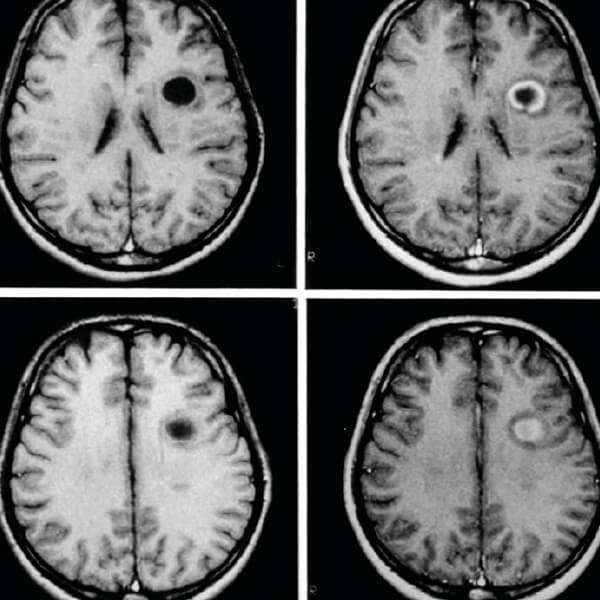
HERSEN-MRI
onthult een volumineuze demyeliniserende laesie, metweefselafbraak in het centrum ("black hole") en contrastopnamedie het doorbreken van de bloed-hersenbarrière en het acutekarakter van de ontsteking aantoont
Deze aanwijzing als ‘doorbraaktherapie’ toont dat tolebrutinib het potentieel heeft om de progressie van de handicap te vertragen en dus te beantwoorden aan een essentiële medische behoefte voor MS-patiënten met een progressieve vorm van de ziekte.De voornaamste bijwerking was een toename van de leverenzymen voorbij 3 keer de bovengrens van de normale waarde, bij 4,1% van de deelnemers (en bij 1,6% in de placebogroep). Al deze gevallen van verhoging van de leverenzymen verdwenen zonder bijzondere medische ingreep.
Er is nu een studie van tolebrutinib aan de gang bij primair progressieve multiple sclerose (PERSEUS). De resultaten daarvan worden verwacht in de tweede helft van 2025.Wat zeker het grote verschil maakt tussen tolebrutinib en de andere behandelingen die momenteel worden gebruikt bij multiple sclerose, is dat het zich niet alleen richt op de adaptieve immuniteit (B-lymfocyten), maar ook op de aangeboren immuniteit die wordt gevormd door de macrofagen en de microgliacellen.

OLIGODENDROCYT-MYELINE-AXONCOMPLEX
Hoofddoelwit van auto-immuniteitbij multiple sclerose
Een ander belangrijk element is het vermogen van het geneesmiddel om het centrale zenuwstelsel binnen te dringen en er lokaal de demyeliniserende letsels aan te pakken.Doordat het zich specifiek op de macrofagen en microgliacellen richt, opent dat zeker nieuwe perspectieven voor de behandeling van multiple sclerose. In de toekomst zouden immunomodulerende en ontstekingsremmende geneesmiddelen mogelijk kunnen samengaan met medicatie die de macrofagen van meet af aan deactiveert. De progressie onafhankelijk van relapsactiviteit (PIRA of Progression Independent of Relapse Activity) zou hiermee heel vroeg vermeden kunnen worden.
Zodoende zouden gelijktijdig de 2 hoofdmechanismen worden geblokkeerd die demyelinisatie veroorzaken: de acute demyelinisatie door de toename van inflammatoire bloedcellen, en de chronische demyelinisatie door de lokale activering van de macrofagen.
Professor Emeritus Christian Sindic
Op de hoogte blijven
Ontvang alle informatie met betrekking tot onderzoek en nieuws van de Charcot Stichting rechtstreeks in je inbox.